水素水サーバーの分類と種別
給水方式
水道直結式
水道管と直結させる方式。吐水と同時に自動で給水。水道管の大がかりな工事が必要
天然水ボトル接続式
天然水入りボトルを接続する方式。水道水より安全で美味しい。ボトル交換の手間がかかる
汲み入れ式
自分の手で水を汲み入れる方式。小型で扱いやすいものの、温水が出せない商品が多い
本体の大きさ
大型
中型
小型
作成方式
電気分解式
水の電気分解を利用。pHや酸素濃度を高上させない工夫が施されている
バブリング
水素を微細な気泡状にして溶け込ませる。水素濃度が高く、かつ低下しにくい
化学反応式
マグネシウムと水の化学反応を利用。ミネラルも摂取できる。水素濃度は低め
浄水方式
活性炭など
逆浸透膜
給水方式と本体の大きさ、作成方式、浄水方式によって分類できる。
給水方式
水道直結式
天然水ボトル接続式
汲み入れ式
本体の大きさ
大型
中型
小型
作成方式
電気分解式
バブリング
化学反応式
浄水方式
活性炭など
逆浸透膜
水道直結式


水道管と直結させる方式。給水は吐水と同時に完全に自動で行われる。
吐水量に制限が無いので、まさに好きな時に好きなだけ飲める。大家族や、料理や手洗いにも使う人、面倒くさがりな人向け。
短所として、大がかりな工事が必要。工事の規模を出来るだけ小さく留めたいなら、設置場所は蛇口の近くになるだろう。
また、工事費が上乗せされるので、初期費用が高い。
本体の大きさは、大型が一般的で、中型以下の商品は見当たらない。
こういった構造上の問題から、設置場所を変えるために移動させるのは大変、というのも短所と言える。
残留塩素を含む水道水を原水とするので、浄水装置の性能は高い。極めて高性能な逆浸透膜を採用する商品も多い。
天然水ボトル接続式


天然水入りの大きなボトルを接続する方式。ボトルが空になったら、自分の手で新しいボトルと付け替える。
天然水には塩素が添加されていないし、長い水道管も通って来ていないので、水道水より安全で美味しい。
浄水処理は既に工場の高性能濾過装置で行われているので、本体に濾材は無く、すなわち濾材交換の作業・費用も無い。
短所として、ボトル交換の手間がかかる。
ボトルの容量は8L・12L・19Lなどで、とても重い。
その上、本体とボトルの接続部が上に位置しているで、重い物を高く持ち上げることになる。よって、食卓の間に置くことを前提とした商品でありながら、女性には向いていない。
ボトル再注文の手続きは、ネットで簡単に行える。商品によっては、定期配達で自動化している。
ボトルの料金は、12Lが1000円、というのが相場。
無くなった場合に市販の天然水や水道水をつぎ足すことは、雑菌の混入やミネラルの沈積による汚染や故障を避けるため、禁止されているか、構造的に不可能になっている。
汲み入れ式



水を自分の手で汲み入れる方式。水道管の大がかりな工事や、重いボトルの交換といった敷居が取り払われている。
入れる水の種類は水道水を前提としているので、浄水機能は備えられている。ただし、水道水を飲用しないことが前提の外国で開発された商品は、例外。
本体の大きさは、小型が一般的で、中型は少数、温水も出せる大型は稀。
他の給水方式と異なり、給水経路が閉鎖されていないので、雑菌や異物の混入の可能性が比較的高い。そこで、清掃しやすくするために、容易に分解できる構造をした商品が多い。また、紫外線やオゾンによる殺菌機能を備えた商品もある。
総じて、初心者向け。
しかし、水素濃度は、作成方式がバブリングの商品で4.0ppm、電気分解のでも高性能なのでは1.6ppmと、妥協の無い商品は多い。
電気分解式

原水を電気分解して水素を発生させ、そのまま水素濃度を高める方式。
水の電気分解
水に二本の電極を浸して電流を流すと、陰極からは水素が、陽極からは酸素が発生する。
陰極 : 4H2O + 4e- → 2H2 + 4OH-
陽極:2H2O → 4H+ + 4e- + O2
両極の総和;4H2O + 4e- + 2H2O → 2H2 + 4OH- + 4H+ + 4e- + O2
結果:2H2O → 2H2 + O2
この結果だけを見ると、水が電気によって酸素と水素に分解されたかのように読み取れる。
問題点として、単純に水を電気分解しただけだと、副産物とみなせる酸素の濃度も上がってしまう。
そこで、水素濃度だけを上げる工夫が施されている。具体的には、電解槽を半透膜で陰極室と陽極室とに隔離して陰極室だけから採水したり、陽極で発生した酸素を電解槽の外へ逃がすなど。
なお、酸素を電解槽の外へ逃がす工夫だと、それで問題は無くなるが、半透膜で隔離する工夫だと、pHが上がってしまう、すなわちアルカリ性に傾いてしまう、という問題が残る。
水素水サーバーで採用されている電解槽は、どちらの問題も解消されたもの。だから、水素濃度だけが高く、かつ中性の水素水が出てくる。
バブリング
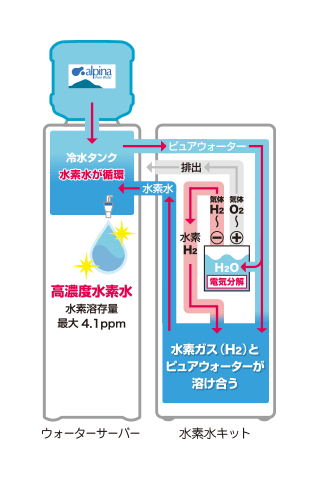
原水を電気分解用水と飲用水の二系統に分け、電気分解で発生させた気体水素を微細な気泡状にして別の経路から飲用水に溶け込ませる方式。ちなみに、バブリング(Bubbling)とは、泡立たせること。
常温常圧の溶解度である1.6ppmを超える水素濃度を実現できる。例として、4.0ppmの商品がある。
また、作成後にグラスなどの開放された容器中で放置しても、水素濃度が低下しにくい。具体的には、普通の水素水なら3時間で半減するところ、バブリングで作成された水素水なら数時間後でもほとんど変わらない。
気泡の大きさが微細なほど、水素が水に溶けやすく、かつ溶けた水素が水中から空気中へ逃げにくくなる。
気泡の大きさに応じた呼び名があり、マイクロバブルやナノバブルと言う。ナノバブルの方が小さく、かつ品質で優れている。
化学反応式

主にマグネシウムと水の化学反応を利用する方式。
マグネシウムと水の化学反応
水中にマグネシウムを入れると、マグネシウムはイオン化して水に溶け、水からは還元された水素が発生する。
Mg + 2H2O →Mg2+ + 2e- + 2H+ + 2OH- →Mg2+ + 2OH-+ H2
Mg2+ + 2OH- ⇆ Mg(OH)2
溶けてマグネシウムイオンになったものの一部は水酸化物イオンとイオン結合し、イオン結晶の水酸化マグネシウムと成って析出する。
水のpHは、溶けているマグネシウムイオンの濃度が高いほど、アルカリ性に傾く。
マグネシウム濃度が高くなる点や、水酸化マグネシムも摂取してしまう点、pHがアルカリ性に傾く点は、長所とも捉えられるが、人によっては短所とも捉えられる。
また、それ以前に、この化学反応の進行速度は、水酸化マグネシウムの常温での溶解度が低いという問題から、かなり遅い。
これらの課題を解消するために、水酸化マグネシウムの濾材としてレジンなどのイオン交換樹脂を取り入れた商品もある。
この手の商品で作成された水素水は、水素濃度が低下しにくいとされている。
また、この手の商品の給水方式は、反応速度が十分に速いので、水道直結式にも対応している。一方で、そうでない商品の構造は、セラミックボールを大量に入れた大きな水槽に、自分で汲み入れた水を溜めておくというものになっていて、汲み足した時には作成に時間がかかる。
両方の商品に残る短所として、マグネシウムなどの原料に寿命があり、消耗部品として定期的な交換が必要な点がある。
ちなみに、製品中のマグネシウムの形態は、無機化合物と共に焼き固めて出来たセラミックとなっている。なお、その他の原料として、複数種の金属を含むセラミックも用いる商品もある。